QM-Handbuch - GUS ERP GmbH
Sie haben die Startseite unseres Qualitätsmanagementhandbuchs geöffnet. Unser Handbuch besteht aus einem öffentlichen und einem nicht öffentlichen Bereich. In dem öffentlichen Bereich können Sie sich nach Belieben bewegen, Links auf den nicht öffentlichen Bereich haben wir mit “nicht öffentlich” gekennzeichnet. Es handelt sich dabei um vertrauliche, weiterführende Informationen über unser Unternehmen und seine Abläufe, deren Zugriff auf unsere Mitarbeiter beschränkt ist.
Ich wünsche Ihnen viel Spaß bei der Lektüre.
(Version 2.2 vom 22.11.2023)
Geltungsbereich
Der Geltungsbereich unseres Qualitätsmanagementsystems erstreckt sich auf alle Prozesse und Organisationseinheiten der
- GUS ERP GmbH
Josef-Lammerting-Allee 20-22
50933 Köln - GUS ERP GmbH – Niederlassung Hamburg
Heidenkampsweg 73
20097 Hamburg - GUS ERP GmbH – Niederlassung München
Claudius-Keller-Str. 3c
81669 München - GUS Schweiz AG
Sonnenstraße 5
9000 St. Gallen
Schweiz
Konformität
Unser Qualitätsmanagementsystem erfüllt die Forderungen der Norm DIN EN ISO 9001:2015
DQS-Zertifikat zum Download
Nicht Anwendbarkeit
Da wir keine zu kalibrierenden Prüfmittel einsetzen, sind die Forderungen aus Punkt 7.1.5 der Norm DIN EN ISO 9001:2015 (Ressourcen zur Überwachung und Messung) für unser Unternehmen nicht relevant und sind nicht anwendbar.
(Version 1.4 vom 16.01.2018)
Wohl kein Industriebereich setzt so hohe Qualitätsanforderungen wie die Unternehmen aus den Branchen Pharma, Nahrungs- und Genussmittel, Chemie, Kosmetik, Biotechnologie und der damit verbundenen Logistik. Die Produkte dieser Unternehmen berühren den unmittelbaren Lebensbereich des Menschen und damit seine Gesundheit, sein Wohlbefinden und seine Lebensqualität.
Deshalb gehen die Anforderungen bei der Entwicklung, Beschaffung, Herstellung, Qualitätskontrolle und Distribution sowie der begleitenden Information weit über die Standards einer Industrienorm wie beispielsweise der ISO 9001:2015 hinaus. Neben den Richtlinien der „Guten Herstellungspraxis“ Good Manufacturing Practice (GMP) sowie verwandter Bestimmungen wie Good Laboratory Practice (GLP), Good Storage Practice (GSP) im Pharma-Bereich stehen zahllose gesetzliche oder amtliche Anforderungen an: Ob nun die Bestimmungen des Arzneimittelgesetzes (AMG), die Arzneimittel- und Wirkstoffherstellungsverordnung (AMWHV) das Kapitel 21 der Codes of Federal Regulations (CFR) oder – für den Food-Bereich – das Lebensmittelhygienegesetz und die EU-Verordnung 178/2002.
Zusätzlich müssen Richtlinien des Handels wie International Food Standard (IFS) und British Retail Consortium (BRC) Global Standard-Food beachtet werden. Diese Rahmenwerke stellen sämtlich die Sorgfalt des Unternehmens und seiner Mitarbeiter in den Mittelpunkt.
Ein wichtiges und von der Industrie anerkanntes Instrument der Qualitätssicherung ist auch die Validierung. Die GUS Group erfüllt hier die Bestimmungen der Arbeitsgemeinschaft Pharmazeutische Verfahrenstechnik (APV), die in der APV-Richtlinie „Computergestützte Systeme“ festgehalten sind.
Unsere Sorgfalt schließt auch die Auswahl von Produktionseinrichtungen und Software-Systemen mit ein. Wir betrachten es als ein Kompliment für die eigene Qualitätsorientierung, dass zahlreiche Unternehmen der Life Sciences Industrien sich für unsere Lösungen als Träger ihrer qualitätsorientierten Geschäftsprozesse entschieden haben. Dabei haben wir uns die Qualitätsvorgaben unserer Kunden zum Maßstab für die Qualitätsziele unserer eigenen Geschäftsprozesse gemacht. Diese Sorgfalt ist in unserer Qualitäts-Charta formuliert und ist damit Verpflichtung für jeden einzelnen Mitarbeiter – und dies bei allen Aufgabengebieten:
- bei Entwicklung und Test von Software-Systemen
- bei der Umsetzung von kundenindividuellen Spezifikationen
- beim Support und der Systemunterstützung im Vertrieb
- bei der Auswahl von Systemkomponenten
- bei der Mitarbeiterqualifikation
- in der Unternehmensorganisation
Engagement, Eigenverantwortung und fachliche Kompetenz des Einzelnen sind die tragenden Säulen unseres Erfolgs. Die Anforderungen und Wünsche unserer Kunden bestimmen dabei unsere Zielsetzungen. Die Organisation unseres Unternehmens mit ihren Strukturen, Zielen und Regelungen schafft das passende Umfeld für eine leistungsfähige Gemeinschaft. Danach ist jeder Einzelne im Rahmen seiner Kompetenzen und Zuständigkeiten für die Ergebnisse der ihm übertragenen Arbeiten verantwortlich.
Qualitätsziele
Für die Lenkung, Analyse und Verbesserung unserer Qualitätsziele haben wir Prozesskennzahlen (nicht öffentlich) definiert und etabliert.
Diese werden regelmäßig erhoben und analysiert. Die Ermittlung der Prozesskennzahlen erfolgt je nach Kennzahl in unterschiedlichen Rhythmen. Die Kennzahlen sind die Grundlage für die monatliche GF-Sitzung. Dort werden die Zahlen analysiert und ggf. steuernde Maßnahmen ergriffen.
(Version 1.3 vom 16.01.2018)
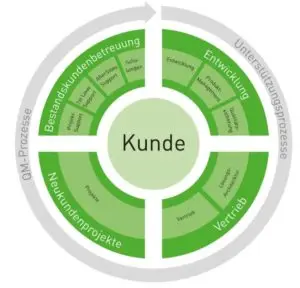
Alle unsere Kernprozesse in den Bereichen
- Entwicklung
- Vertrieb
- Neukundenprojekte
- Bestandskundenbetreuung
fokussieren auf unsere Kunden. In folgende Grafik erhalten Sie Informationen über unsere Prozesse:
(Version 1.4 vom 13.02.2012)
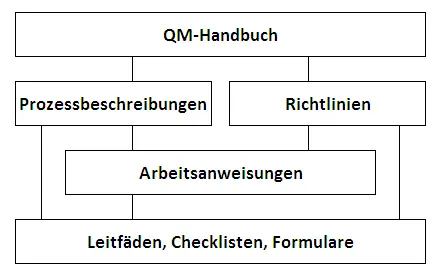
Struktur der QM-Vorgabedokumentation
Die Vorgabedokumentation unseres Managementsystems besteht neben diesem Management-Handbuch aus Prozessbeschreibungen, Richtlinien, Arbeitsanweisungen und Checklisten (nicht öffentlich), die Prozessabläufe beschreiben und Vorgaben zu deren ordnungsgemäßen Durchführung beinhalten. Weiterhin wird in diesen Dokumenten auf mitgeltende Formulare, Checklisten und Leitfäden (nicht öffentlich) verwiesen. Alle QM-Vorgabedokumente sind mit Revisionsstand eindeutig identifizierbar.
Aktualisierung, Prüfung und Freigabe der QM-Vorgabedokumentation
Verantwortlich für die Aktualisierung der QM-Vorgabedokumentation sind die jeweiligen Prozessverantwortlichen. Für die Unterschriftenregelung zu QM-Vorgabedokumenten gilt:
⇒ Erstellung ⇒ Autor
⇒ Prüfung ⇒ Prozesseigner, Prozessmitwirkung, QM-Beauftragter
⇒ Freigabe ⇒ Sprecher der Geschäftsführer
Die Lenkung der QM-Vorgabedokumente (nicht öffentlich) erfolgt durch den Organisationsbereich QM. Dieser stellt sicher, dass die jeweils gültige Version der Vorgabedokumentation allen Mitarbeitern des Unternehmens zur Verfügung steht und bekannt ist. Jedes QM-Vorgabedokument behält grundsätzlich stets seine Gültigkeit bis zur offiziellen Freigabe einer neuen Version oder einer Rückziehung des Dokumentes. Auch die beabsichtige Optimierung und/oder Änderung eines Prozesses unterliegt den Vorgaben freigegebener QM-Vorgabedokumente, d.h. der Anwendung bestehender Regeln. In Abstimmung mit dem QM-Beauftragten kann ein Prozessverantwortlicher jedoch ein Pilotprojekt und/oder eine Ausnahme definieren, die nicht den bestehenden Regularien unterworfen wird. Dies bindet jedoch ausnahmslos an die schriftliche Freigabe des QM-Beauftragten. Sollte es im Einzelfall einmal nicht möglich sein, bestehende Regeln anzuwenden (z.B. weil eine Situation in der Vorgabe nicht berücksichtigt ist), ohne dass dies mit dem QM-Beauftragten abgestimmt werden kann (z.B. wegen einer notwendigen kurzfristigen Entscheidung), so ist dies durch den Prozessverantwortlichen schriftlich mit Angabe der Ausgangslage und den Überlegungen, die zur Abweichung geführt haben bzw. führen werden, zu dokumentieren und dem QM-Beauftragten zu übermitteln.
Herausgabe von QM-Vorgabedokumenten
Das QM-Handbuch ist öffentlich und darf als Kopie an Kunden und andere interessierte Parteien weitergegeben werden. Es handelt sich dabei jedoch ausschließlich um Informationsexemplare, welche nicht dem laufenden Änderungs- und Austauschdienst unterliegen. Sie entsprechen nur bei ihrer Herausgabe dem aktuellen Stand. Andere Dokumente, wie zum Beispiel Prozessbeschreibungen und Arbeitsanweisungen (nicht öffentlich), beinhalten Know-how unseres Unternehmens und sind daher vertraulich zu behandeln. Ihre Herausgabe an Stellen außerhalb unseres Unternehmens bedarf in jedem Einzelfall der Genehmigung durch die Unternehmensleitung.
Daten und Aufzeichnungen
In unserer QM-Vorgabedokumentation sind Art und der Umfang notwendiger Aufzeichnungen vorgegeben. Prüfergebnisse werden zu den jeweiligen Prozessen und Produkten aufgezeichnet. Solche Aufzeichnungen dienen dem Nachweis der durchgeführten Prüfung sowie der Dokumentation der Ergebnisse. Diese Nachweise werden regelmäßig durch die Prozessverantwortlichen ausgewertet, um Hinweise auf Veränderungen und Schwachstellen in der Organisation zu erhalten.
(Version 1.3 vom 16.01.2018)
Planung und Steuerung
Zu Beginn des Geschäftsjahres werden die erfolgskritischen Rahmenparameter der Unternehmenskennzahlen der letzten Jahre analysiert. Darauf aufbauend wird zusammen mit der erwarteten Marktentwicklung ein Plan für das kommende Geschäftsjahr erstellt. Dieser wird zusammen mit den Planparametern auf die einzelnen Monate heruntergebrochen. Diese Planzahlen und Planparameter sind die Grundlage für die monatlich, im Rahmen des Geschäftsführer-Meetings, stattfindende SOLL-IST-Analyse. Im Rahmen dieser Analyse werden alle wirtschaftlichen und Performance beeinflussende Kenngrößen aufbereitet und einer umfangreichen Analyse unterzogen. Dies versetzt die GUS in die Lage kurzfristig auf Änderungen am Markt zu reagieren und schnell die notwendigen Maßnahmen zur Unternehmenssteuerung zu ergreifen.
Prozesskennzahlen
Für die Lenkung, Analyse und Verbesserung unserer Qualitätsziele haben wir Prozesskennzahlen (nicht öffentlich) definiert und etabliert. Diese werden regelmäßig erhoben und analysiert. Die Ermittlung der Prozesskennzahlen erfolgt je nach Kennzahl in unterschiedlichen Rhythmen. Die Kennzahlen sind die Grundlage für die monatliche GF-Sitzung. Dort werden die Zahlen analysiert und ggf. steuernde Maßnahmen ergriffen. In regelmäßigen Management-Reviews werden kaufmännische und qualitätsrelevante Daten des Unternehmens analysiert und diskutiert, welche Rückschlüsse auf die Leistungsfähigkeit der Prozesse des Unternehmens zulassen. Eingaben für das Management-Review sind:
- Ergebnisse von internen Audits,
- Ergebnisse von Lieferantenaudits,
- Rückmeldungen von Kunden (Meldungen an die Hotline),
- Prozesskennzahlen,
- Wirtschaftliche Kennzahlen
- Soll-Ist-Vergleiche mit den Plandaten
- Status von Vorbeugungs- und Korrekturmaßnahmen,
- Änderungen, die sich auf das Managementsystem auswirken,
- Empfehlungen für Verbesserungen.
- Rückmeldungen der relevanten interessierten Parteien
- Ergebnisse von Überwachungen und Messungen
- Leistungen von externen Anbietern
Bei Auffälligkeiten werden geeignete Maßnahmen eingeleitet, um so zeitnah wie möglich auf die festgestellten Schwachpunkte im Unternehmen zu reagieren. Die Ergebnisse und Festlegungen der Bewertung werden protokolliert und an die Verantwortungsträger kommuniziert. Die Umsetzung vereinbarter Maßnahmen wird vom Qualitätsbeauftragten und dem Führungskreis überwacht.
Interne Audits
In internen Audits (nicht öffentlich) überprüfen wir regelmäßig die Umsetzung unserer Vorgaben in die Praxis und die Kenntnis der Mitarbeiter über die ihre Arbeit betreffenden Regelwerke. Besonderes Augenmerk liegt dabei auf der Erarbeitung von Prozessoptimierungen; hierzu können unsere Mitarbeiter aus ihrer praktischen Arbeit heraus wertvolle Hinweise geben. Audits werden systematisch geplant und von geschultem, kompetentem Personal durchgeführt. Die Ergebnisse interner Audits werden dokumentiert. Abweichungen von den Vorgaben und erkannte Schwachstellen werden mit entsprechenden Maßnahmen unterlegt, um die Ursachen zu beseitigen. Die Wirksamkeit von solchen Korrektur- und Vorbeugemaßnahmen wird in Folgeaudits überprüft.
(Version 2.3 vom 22.11.2023)
Die Überprüfung unseres Managementsystems erfolgt durch mehrere voneinander unabhängige Kontrollverfahren und -Instanzen.
Lieferantenaudits
In Lieferantenaudits überprüfen Kunden und Interessenten unser Qualitätsmanagementsystem. Immer mehr Firmen insbesondere aus der pharmazeutischen Industrie folgen dabei den Empfehlungen des GAMP-Leitfadens, der den pharmazeutischen Unternehmen die Durchführung von Lieferantenaudits ausdrücklich empfiehlt. Da wir ständig an der Optimierung unserer Prozesse arbeiten, sind gerade Hinweise externer Überprüfungen besonders wertvoll, unterliegen sie doch nicht der uns naturgemäß gegebenen „Betriebsblindheit“. Aus Lieferantenaudits haben wir zahlreiche Anregungen zur Prozess- und Qualitätsoptimierung erhalten und erfolgreich umsetzen können.
Ergebnisse aus Lieferantenaudits (Auszüge)
19.04.2023 BGS Beta Gamma Service GmbH & Co. KG
Conclusion: The supplier GUS ERP GmbH remains an approved supplier of BGS.
11.11.2021 G. Pohl-Boskamp GmbH & Co. KG
Das Audit hat ergeben, dass die GUS ERP GmbH ein gut funktionierendes Qualitätsmanagement betreibt und weitreichende Erfahrungen mit den Anforderungen an die Softwareeinführung im GMP-regulierten Umfeld hat. Die Prozesse sind umfassend dokumentiert.
21.11.2019 medac GmbH / oncomed manufacturing a.s.
Die Freigabe der GUS Group als qualifizierter Lieferant und Dienstleister wird empfohlen.
03.09.2019 Medios Manufaktur GmbH
– Die GUS ERP GmbH unterhält ein sehr gut funktionierendes nach ISO 9001:2015 zertifiziertes Qualitätsmanagementsystem.
– Die Audit-Ergebnisse bestätigen die sehr hohe Fachkompetenz der Mitarbeitenden im Rahmen der Softwareentwicklung und -validierung im GxP-regulierten Umfeld.
– Bereits in der Projektphase zur Einführung der GUS-OS ERP-Software konnte die GUS ERP GmbH mit ihrer langjährigen Erfahrung in der Softwareeinführung in der pharmazeutischen Industrie überzeugen.
19.07.2019 Pharmpur GmbH
GUS services Pharmpur GmbH in the preparation of an ERP system for Pharmpur ́s business processes. The company is very well suited for this purpose. GUS demonstrated to have a very good quality management system in place. The system is based on ISO9001:2015. Pharmaceutical processes are known to GUS.
22.11.2016 Wagener & CO. GmbH
Während des Audits, der ausgeführten Gespräche und der späteren Prüfung der beiliegenden Dokumente lagen keinerlei Gründe vor, die GUS nicht als Lieferant für GMP-relevante Software einzusetzen.
27.09.2016 Schaper & Brümmer
Auf Grund der positiven Auditergebnisse wird die Freigabe der GUS ERP GmbH als ein qualifizierter Lieferant für die Entwicklung, die Einführung und die Wartung des ERP-Systems GUS-OS Suite durch die Auditoren […] empfohlen. […]
Die GUS ERP GmbH betreibt ein gut funktionierendes QM-System nach ISO 9001 :2008, welches stichprobenartig geprüft wurde. […]
Die Audit-Ergebnisse belegen die notwendigen Erfahrungen und GMP-Kompetenz des Unternehmens für die Entwicklung, die Einführung und die Wartung der OS-ERP Software. […]
Das Unternehmen konnte auch aufzeigen, das umfangreiche Erfahrungen im Bereich der pharmazeutischen Industrie die Kompetenz untermauern.
02.02.2016 aniMedica
Zusammenfassung / Bewertung
Die GUS stellte sich im Rahmen des Audits als sehr strukturiertes Unternehmen dar. Aufgrund von langjährigen Erfahrungen im GMP-Bereich durch vorangegangene Projekte und den vorliegenden Inspektionsergebnisse, entspricht die GUS den Anforderung des Anhangs 11 „Computergestützte System“ des EU-GMP-Leitfadens sowie den Anforderungen des Aide-Memoire „Überwachung computergestützter Systeme“ des ZLGs vollumfänglich und kann somit als qualifizierter Lieferant einer ERP-Software eingestuft.
24.06.2015 Medac
Im durchgeführten Audit zur Requalifizierung der GUS präsentierte sich das Unternehmen mit einem starken Fokus auf das Qualitätsmanagementsystem. […]. Insgesamt ist ein sehr positiver Gesamteindruck entstanden. Die GUS hat ihre Qualitätsprozesse erweitert und weiter optimiert.
Alle Auditteilnehmer haben die angefragten Informationen umgehend zur Verfügung gestellt sowie ausführlich erläutert. Die angeforderte Dokumentation stand vollständig zur Verfügung.
Die GXP-Konformität ist weiterhin gegeben. Die im letzten Audit beleuchtete FDA-Compliance wurde stichpunktartig beleuchtet und konnte an diesen Punkten bestätigt werden. […]
04.03.2015 Excella
Die GUS Group AG & Co KG besitzt umfangreiche Projekt- und Auditerfahrung imGxP regulierten Markt.
Formal hat das Audit bestätigt, dass die Anforderungen an die Softwareentwicklung im Rahmen von Implementierungsprojekten gemäß der Guten Praxis und den Forderungen des ISPE GAMP5 erfüllt sind.
Darüber hinaus verfügt das Projektpersonal über gute Kenntnis der GMP. Das QM System ist gut dokumentiert erwies sich als fähig, den Prozess der Softwareentwicklung abzubilden und insbesondere die Rückverfolgbarkeit zu gewährleisten. Die formale Korrektheit der Arbeitsweise lässt indes nicht zwingend einen Rückschluss auf eine insgesamt erfolgreiche Projektabwicklung zu.
03.12.2014 Protina
Der Audit wurde in einer positiven Atmosphäre durchgeführt.
Das Audit wurde sehr gut vorbereitet. Die Einführung in das Audit war gut strukturiert.
Die Ergebnisse belegen die notwendigen Erfahrungen und GMP — Kompetenz des Unternehmens für die Entwicklung, die Einführung und die Wartung der OS-ERP Software.
Das Unternehmen GUS Group konnte im Audit aufzeigen, dass in den letzten Jahren Kunden aus der GMP — regulierten Industrie erfolgreiche Audits durchgeführt haben. Das Unternehmen konnte aufzeigen, das umfangreiche Erfahrungen im Bereich der pharmazeutischen Industrie die Kompetenz untermauern. Es konnte aufgezeigt werden, dass erste Projekte bei pharmazeutischen Unternehmen mit Medizinprodukten erfolgreich realisiert wurden.
Die Mitarbeiter haben eine langjährige Erfahrung im GxP Markt, ein hohes Verständnis für die Validierungsanforderungen und Identifikation mit dem Unternehmen.
Das Unternehmen GUS ist im Vergleich mit dem ERP — Markt (DACH) sehr gut zu den Anforderungen der GxP regulierten Industrie positioniert.
08.06.2014 BAG
Das durchgeführte Lieferantenaudit bei der GUS ERP GmbH, Standort Köln hat gezeigt, dass die auditierten Bereiche
- Qualitätsmanagement System
- Softwareentwicklungsprozess
- Testverfahren
- Support und Wartung
- FDA 21 CFR Part 11 Compliance
die im ISPE GAMP5 Leitfaden aufgestellten Grundsätze und Vorgaben erfüllt.
Das Lieferantenaudit bestätigt zudem, dass die GUS ERP GmbH über die notwendigen Erfahrungen im GxP Umfeld verfügt und die Entwicklung, Einführung und Wartung der GUS OS Suite Software nach geltenden regulatorischen Vorgaben erfolgt.
Einer weiteren Zusammenarbeit steht aus Sicht des Auditors nichts entgegen.
22.08.2013 Lichtenheldt
Das Audit bei der GUS ERP GmbH, Standort Köln verlief erfolgreich.
Gesamturteil: GUT
Der weiteren Zusammenarbeit steht aus Sicht der Auditoren nichts entgegen.
21.03.2013 Stoma
[…]Die Ergebnisse belegen die notwendigen Erfahrungen und GMP – Kompetenz des Unternehmens für die Entwicklung, die Einführung und die Wartung der OS-ERP Software. Das Unternehmen konnte im Audit aufzeigen, dass in den letzten Jahren Kunden aus der GxP – regulierten Industrie erfolgreiche Audits durchgeführt haben. Das Unternehmen konnte aufzeigen, das umfangreiche Erfahrungen im Bereich der pharmazeutischen Industrie die Kompetenz untermauern. […]
Die Mitarbeiter haben eine langjährige Erfahrung im GxP Markt, ein hohes Verständnis für die Validierungsanforderungen und Identifikation mit dem Unternehmen. Das Unternehmen GUS ist im Vergleich mit dem ERP -Markt (DACH) sehr gut zu den Anforderungen der GxP regulierten Industrie positioniert.
31.07.2012 BGS
Fazit: Der sehr gute Endruck, der während der Angebots- und Projektphase gewonnen wurde, hat sich im Audit bestätigt. Stärke: GUS pflegt und lebt ein angemessenes und gut dokumentiertes Qualitätsmanagementsystem, bei dem Aufwand und Nutzen in einem sehr guten Verhältnis zu stehen scheinen. Es wurden keine Abweichungen festgestellt. GUS sollte als Lieferant für das qualitätsrelevante Produkt ERP-System GUS-OS zugelassen werden.
> Auditbericht (nicht öffentlich)
01.12.2011 Steigerwald
Die Implementierung von gesicherten Prozessen – initiiert durch die Zertifizierung – insbesondere in den Bereichen Produktentwicklung und Projektdurchführung zeigt, dass das Unternehmen eine aktive Qualitätspolitik betreibt und nicht nur auf Kundenanforderungen reagiert. […]
Die Auditoren haben den Eindruck gewonnen, dass das vorgestellte Qualitätssicherungssystem gelebt und in allen relevanten Bereichen der Firma umgesetzt wird. […]
In Bezug auf den Einsatz von Standard- Lösungen im pharmazeutischen GxP-Bereich sowie die damit verbunden Dienstleistungen wird die Fa. GUS als Qualifizieter Lieferant eingestuft.
> Auditbericht (nicht öffentlich)
23.11.2011 bela-pharm GmbH & Co. KG
Das Audit konnte in einer offenen und freundlichen Atmosphäre durchgeführt werden. Die verlangten Informationen standen kurzfristig bereit und das Personal stand für Fragen kompetent zur Verfügung. Das QM-System der GUS hat einen durchdachten und transparenten Eindruck gemacht. Die besonderen Anforderungen des pharmazeutischen Umfeldes waren offensichtlich bekannt und wurden entsprechend erfüllt.
> Auditbericht (nicht öffentlich)
07.06.2011 Tillots Pharma AG
The audit team received confirmation that GUS has anextensive and well-applied Quality System in place. Development methods and testing standards are defined and applied. Product release follows predefined methods. Change control and configuration management are handled skillfully. Document review and approval is clearly established for QMS documentation.
> Auditbericht (nicht öffentlich)
19.06.2009 AvidiaMed
Die Stärken der GUS liegen sicherlich in der seit langen Jahren konsequenten Ausrichtung auf Qualität. Das Qualitätsbewusstsein und das damit verbundene QM-System sind kontinuierlich weiterentwickelt und verinnerlicht worden. Dass der Nutzen von Qualität erkannt und umgesetzt worden ist, konnte während des gesamten Audits durch die Mitarbeiter und die Führung nachhaltig vermittelt werden. Die Ausrichtung auf Qualität wurde am aktuellen QM-System und an der Tool-gestützten Dokumentation der System- und Entwicklungstests (durch z. B. VALREP) demonstriert. Das Audit hat bestätigt, dass die GUS entsprechend den GxP-Anforderungen Software entwickelt und Dienstleistungen erbringt.
> Auditbericht (nicht öffentlich)
17.02.2009 SANIPharma GmbH
Das Qualitätsmanagementsystem der GUS ERP GmbH ist vorbildlich und auf einem hohen Niveau geführt. Dies zeigt sich u.a. an den regelmäßigen Zertifizierungen nach DIN EN ISO 9001, sowie der Transparenz und Souveränität die während des Audits seitens der GUS bestand. Keine Korrekturmaßnahmen erforderlich.
> Auditbericht (nicht öffentlich)
18.08. – 21.08.2008 medac Gesellschaft für klinische Spezialpräparate GmbH
Results Overall assessment:
GUS Development Lifecycle processes and procedures are VERY GOOD
GUS staff are all competent, good listeners, open to change, know their business
GUS Team appears to be committed to the overall success of the joint Medac/GUS Project
auditors feel that GUS has the ability to compete in the US market (and worldwide)
Pluses
- Training Documentation availability on the intranet
- Configurability of the system
- Audit trail functionality
- Cross functionality
- Visualization of BOM level to review status, deviations, etc.
- Quality Systems
- Ability to generate the documentation of roles, workflows, etc needed for IQ
- Real-time database for capturing errors and problems
Assessment documents were generated in the following areas:
Review of Quality Systems, Development and Production Life Cycle Supporting GUS-OS ERP
21 CFR Part 11 Assessment (Electronic Records/Signature) for GUS OS ERP
GMP suitability of GUS OS ERP software functional requirements
> Auditbericht (nicht öffentlich)
20.11.2007 Parexel
The GUS group is trusted providing software with high quality. The company is also trustedto deliver appropriate services to its customers, and to continue to do so in future. This isproven by the company’s history, the large customer basis, the high number of installations,and the loyalty of customers.
The staff is trusted to be competent, knowledgeable, and well trained as proven by (most) personal files.The Quality Management system including the QM handbook and all documentedprocedures were impressively presented. The ISO certification provides evidence that this is agreed by certifiers.
> Auditbericht (nicht öffentlich)
13.06.2007 Hennig Arzneimittel GmbH
„Während des Audits vermittelten die Unternehmensführung, alle direkt und indirekt beteiligten Mitarbeiter aus Entwicklung, Projekt und Service absolute Kenntnis und Anwendung des QM Systems und dass dies auch wirklich gelebt wird.
Folgende Ergebnisse aus diesem Audit sind festzuhalten:
- Stärke des Unternehmens:
Die Stärken der GUS liegen sicherlich in der seit langen Jahen konsequenten Ausrichtung auf Qualität. Das Qualitätsbewusstsein und damit verbundene QM System ist gewachsen und verinnerlicht worden. Hier ist der Nutzen von Qualität erkannt und umgesetzt worden. Dies ist während des gesamten Audits am aktuellen QM System, den auch selbst genutzten Tools (z.B. VALREP) sowie bei den Mitarbeitern und der Führung nachhaltig vermittelt worden. Das Audit hat bestätigt, dass die GUS GMP compliant Software entwickelt und Dienstleitungen erbringt. - Verbesserungs-/Empfehlungspotential:
Im Zuge des Audits wurden keine nennenswerten Schwächen erkannt.
> Auditbericht (nicht öffentlich)
03.08.2006 Bombastus-Werke AG
„Die GUS ERP GmbH konnte belegen, dass das GUS-OS ERP-System unter der Anwendung eines ausgereiften Qualitätsmanagementsystems entwickelt wurde.
Das Qualitätsmanagementsystem deckt die GMP-Anforderungen an die Entwicklung von Software ab.
Ein signifikanter Faktor für die Qualität sind der ausgeprägt hohe Grad der Qualifizierung und Erfahrung der Mitarbeiter, die untypisch lange Branchenerfahrung und die Referenzen in der Pharmazeutischen Industrie.”
> Auditbericht (nicht öffentlich)
03.03.2006 Interessent
„Das im Rahmen dieses Audits vorgestellte Qualitätsmanagement-system ist geeignet, eine nachvollziehbare Softwareentwicklung zu gewährleisten, Fehler und deren Behebung nachvollziehbar zu dokumentieren und gelenkt abzuarbeiten und eine sachgerechte, weitestgehend vorbereitete Einführung der Software GUS-OS ERP beim Kunden zu ermöglichen.”
„Insbesondere ist bei GUS-OS ERP hervorzuheben, dass die Validierungsaktivitäten des Kunden durch eine umfangreiche, bereits im Rahmen der Entwicklung erstellte Testdokumentation, sowie ein validiertes Dokumentationstool VAL-REP zur Aufzeichnung der Testfälle unterstützt werden.”
„Es wurden im Audit keine kritischen und schwerwiegenden oder sonstigen Mängel festgestellt.”
> Auditbericht (nicht öffentlich)
07.12.2005 Riemser Arzneimittel AG
„Die GUS hat ein QM-System installiert, das geeignet ist, die Erstellung von Software für den pharmazeutischen Bereich, die den Anforderungen an GMP entspricht, sicherzustellen.”
„Besonders hervorgehoben werden sollen die großen Anstrengungen, die die GUS Group unternommen hat, um beim GUS-OS ERP die Anforderungen der pharmazeutischen Industrie nach Dokumentation und Validierbarkeit eines solchen Programms zu erfüllen. Ebenso die vielfältigen Hilfen, die diesen Firmen bei der Validierung inzwischen angeboten werden können.”
„Die GUS Group kann als Softwarelieferant für den pharmazeutischen Bereich freigegeben werden.”
> Auditbericht (nicht öffentlich)
Jährliche Begutachtung zur Systemförderung
Einmal jährlich überprüft die DQS in einer „Begutachtung zur Systemförderung“ unser Qualitätsmanagementsystem. Dabei werden das Qualitätsmanagementsystem, die Dokumentenlenkung (nicht öffentlich), die Umsetzung der Vorgaben in die Praxis und die Kenntnis der Mitarbeiter über Prozessbeschreibungen (nicht öffentlich), Vorgaben und Richtlinien überprüft. Auch hieraus haben wir zahlreiche Anregungen zur Prozess- und Qualitätsoptimierung erhalten und erfolgreich umsetzen können.
> DQS-Zertifikat zum Download
Gutachten
Zur Verifizierung von Entwicklungsarbeiten und Aufgaben des Prozessmanagements beauftragen wir in unregelmäßigen Abständen externe Sachverständige zur Erstellung von Gutachten. Insbesondere mit der Neueinführung der GUS-OS Lösungsfamilie wurden die Entwicklungsprozesse und Kundenprojekte einer ausführlichen externen Überprüfung unterzogen.
(Version 1.3 vom 16.01.2018)
Bewertung des Managementsystem
Grundlage der Bewertung der Kennzahlen und Informationen unseres Unternehmens sind die Ziele unseres Unternehmens beziehungsweise der Vergleich mit Zahlen aus vorangegangenen Berichts- und Bewertungsperioden sowie den Plandaten. Bei Fehlerhäufungen, tendenzieller Verschlechterung der Ergebnisse sowie im Rahmen unserer Aktivitäten zur kontinuierlichen Verbesserung werden Maßnahmen eingeleitet, um die Ursachen von Fehlern oder Verschlechterungen zu beseitigen. Die Bewertung des Managementsystems findet auf mehreren Ebenen statt: Bewertung durch den Führungskreis (Management-Reviews)In regelmäßigen Management-Reviews werden kaufmännische und qualitätsrelevante Daten des Unternehmens analysiert und diskutiert, welche Rückschlüsse auf die Leistungsfähigkeit der Prozesse des Unternehmens zulassen. Eingaben für das Management-Review sind:
- Ergebnisse von internen Audits,
- Ergebnisse von Lieferantenaudits,
- Rückmeldungen von Kunden (Meldungen an die Hotline),
- Prozesskennzahlen,
- Wirtschaftlichen Planzahlen,
- Soll-Ist-Vergleiche mit den Plandaten,
- Status von Korrektur- und Vorbeugungsmaßnahmen,
- Änderungen, die sich auf das Managementsystem auswirken,
- Empfehlungen für Verbesserungen.
- Rückmeldungen der relevanten interessierten Parteien
- Ergebnisse von Überwachungen und Messungen
- Leistungen von externen Anbietern
Bei Auffälligkeiten werden geeignete Maßnahmen eingeleitet, um so zeitnah wie möglich auf die festgestellten Schwachpunkte im Unternehmen zu reagieren. Die Ergebnisse und Festlegungen der Bewertung werden protokolliert und an die Verantwortungsträger kommuniziert.Die Umsetzung vereinbarter Maßnahmen wird vom Qualitätsbeauftragten und dem Führungskreis überwacht.
Bewertung durch die Oberste Leitung
Eine formale Bewertung unseres Managementsystems führen wir einmal jährlich durch. Grundlage hierfür ist der Bericht des Qualitätsmanagementbeauftragten. Eingaben für seinen Bericht sind:
- Ergebnisse von internen Audits (nicht öffentlich),
- Ergebnisse von Lieferantenaudits,
- Rückmeldungen von Kunden und Meldungen an die Hotline,
- Prozesskennzahlen (nicht öffentlich).
Ferner enthält der Bericht Informationen über
- Status von Korrektur- und Vorbeugungsmaßnahmen,
- Änderungen, die sich auf das Managementsystem auswirken,
- Empfehlungen für Verbesserungen.
Die Ergebnisse und Festlegungen der Bewertung werden protokolliert und an die Verantwortungsträger kommuniziert. Die Umsetzung vereinbarter Maßnahmen werden vom Qualitätsmanagementbeauftragten und dem Führungskreis überwacht.
Korrektur- und Vorbeugungsmaßnahmen
Die Lenkung und Überwachung von Korrektur- und Vorbeugungsmaßnahmen (nicht öffentlich) erfolgt durch den Organisationsbereich QM.
Korrekturmaßnahmen
Durch die regelmäßige Beobachtung und Auswertung der in Prüfungen ermittelten Daten werden Mängel in der Organisation frühzeitig erkannt. Die Verantwortlichen der Fachbereiche haben die Pflicht, systematische Mängel im Rahmen ihrer Zuständigkeit und Kompetenz zu ermitteln und umgehend abzustellen bzw. diese an ihre Vorgesetzten zu melden. Fehlerhäufungen werden ermittelt, die Ursachen werden durch angemessene Maßnahmen abgestellt. Kleine Korrekturmaßnahmen werden durch die Verantwortlichen direkt und unbürokratisch umgesetzt. Umfangreiche Korrekturmaßnahmen, bei denen z.B.
dem wiederholten Auftreten kritischer Fehler entgegengewirkt werden soll,
bereichs- oder unternehmensübergreifende Maßnahmen notwendig sind,
weitreichende Investitions- oder Organisationsentscheidungen zu erwarten sind,
werden mit der Führungsebene abgestimmt. Je nach Umfang der Maßnahmen werden diese systematisch geplant, dokumentiert und umgesetzt. Korrekturmaßnahmen, welche bestehende Regelungen unseres Unternehmens betreffen, werden entsprechend in die Dokumentation unseres Managementsystems eingepflegt. Die Wirksamkeit von Korrekturmaßnahmen wird überprüft.
Vorbeugungsmaßnahmen
Vorbeugungsmaßnahmen werden eingeleitet, um zu erwartende Risiken in Produkten oder Prozessen bzgl. der qualitätsrelevanten Auswirkungen zu minimieren oder auszuschalten, bevor Probleme entstehen. Sie basieren auf den Erfahrungen aus bekannten, vergleichbaren Prozessen und Verfahren und fließen in die Planung und Entwicklung neuer Produkte sowie die Verbesserung bestehender Prozesse oder Verfahren ein. Die Wirksamkeit von Vorbeugungsmaßnahmen wird überprüft.
(Version 1.2 vom 25.10.2013)
Der Qualitätsmanagementbeauftragte ist ausgestattet mit der Befugnis, über alle qualitätsrelevanten Aktionen bezüglich unseres Qualitätsmanagementsystems zu entscheiden. Er hat die Aufgabe, unser nach der Norm DIN EN ISO9001 zertifiziertes QM-System aufrechtzuerhalten und weiter zu entwickeln. Ferner ist er verantwortlich für die Kontrolle einer effizienten Umsetzung der qualitätsrelevanten Anweisungen. Außerdem obliegt ihm die Schulung der Mitarbeiter, um sie für die Belange des Qualitätsmanagements zu sensibilisieren. Der Qualitätsbeauftragte handelt in seinem Verantwortungsbereich frei von Weisungen und unabhängig von Vorgesetzten. Aufgaben:
- Aufbau, Aufrechterhaltung und Weiterentwicklung des Managementsystems nach DIN EN ISO9001
- Prüfung von QM-Vorgabedokumenten (Erstellung durch die Prozessowner)
- Fortschreibung und Überwachung von Korrektur- und Vorbeugemaßnahmen (Erarbeitung durch Prozessowner)
- Durchführung von Lieferantenaudits
- Durchführung interner Audits
- Schulung der Mitarbeiter zum QM-System
- Ernennungsurkunde QM-Beauftragter (nicht öffentlich)
(Version 1.7 vom 04.06.2024)
QM-Handbuch der GUS
Die Unternehmensleitung der GUS ERP GmbH setzt dieses Handbuch mit dem heutigen Tag in Kraft und legt fest, dass die darin enthaltenen Anweisungen sowie zugehörige Dokumente für die Mitarbeiter des Unternehmens verbindlich sind.
Köln, den 04.06.2024
Thorsten Schlechtriem, CEO der GUS ERP GmbH